Что необходимо предпринять при мутации редуктазы метионинсинтазы
Содержание
Почему повышен уровень гомоцистеина в крови? Лечение при генетических мутациях в MTHFR, MTR, MTRR
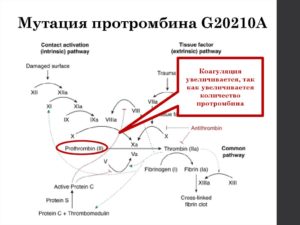
Гомоцистеин — это серосодержащая аминокислота, которая образуется при метаболизме белка.
Впервые она была обнаружена в камне мочевого пузыря в 1933 году американским биохимиком Винсентом дю Виньо. Гомоцистеин образуется в результате метаболизма пищевого метионина, который содержится в животных белках.
Гипергомоцистеинемия — повышение уровня гомоцистеина в крови, которое может способствовать повреждению артерий и образованию тромбов в ваших кровеносных сосудах (например, тромбоз глубоких вен и тромбоэмболия легочной артерии).
Имеются эпидемиологические данные, свидетельствующие о связи между повышением гомоцистеина и нейродегенеративными состояниями, включая болезнь Альцгеймера, болезнь Паркинсона и инсульт. Повышенный уровень гомоцистеина снижает доступность АТФ для нейронов и вызывает тяжелое повреждение нервной системы.
Сывороточный гомоцистеин может служить биомаркером, используемым для оценки метилирования.
Референсные интервалы
Нормальный уровень гомоцистеина в крови составляет менее 15 микромолей на литр (мкмоль/л) крови. Повышение концентрации гомоцистеина может быть:
Умеренное: 15-30 мкмоль/л
Среднее: 30-100 мкмоль/л
Тяжелое: более 100 мкмоль/л
Причины повышения гомоцистеина
Концентрация гомоцистеина может увеличивается с возрастом. Ниже перечислены основные причины повышения гомоцистеина.
Генетические факторы
Повышение гомоцистеина может быть вызвано генетическими дефектами ферментов, которые участвуют в метаболизме гомоцистеина. Организм человека содержит более 50 триллионов клеток, и каждая клетка содержит полный набор инструкций для вас. Инструкции закодированы в вашей ДНК. Короткие сегменты ДНК называются генами.
Ваша ДНК — «кулинарная» книга, ваши гены — рецепты. Гены кодируют определенные белки, и эти белки играют решающую роль в функционировании тканей и органов организма. У людей около 20 000 генов. Среди этих 20 000 генов находятся гены MTHFR, MTR, MTRR, CBS. У большинства людей есть две копии этих генов.
Ген MTHFR необходим, чтобы сделать фермент метилентетрагидрофолатредуктазу. Когда вы едите продукты, которые содержат фолиевую кислоту (витамин B9), фермент метилентетрагидрофолатредуктаза превращает ее в метилфолат, активную форму фолата. Метилфолат является ключевым игроком в метилировании, процессе добавления метильной группы к химическому соединению.
Метилирование является основополагающим для правильного функционирования почти всех систем организма.Купить метилфолат →
Метилфолат участвует:
- В восстановлении и регенерации ваших клеток, тканей и ДНК.
- Регуляция экспрессии генов и белков.
- В синтезе нейротрансмиттеров, которые влияют на настроение, сон, поведение, познание и память.
- В контроле гомоцистеина.
- Сдерживает воспаление под контролем.
- Помогает вашей печени в переработке жиров.
- В активации и регулировании иммунной системы.
Что делать при мутации в гене MTHFR? Метилирование чрезвычайно важно!
Те из нас, у кого есть мутации в гене MTHFR (A1298C или C677T), имеют дефектный фермент метилентетрагидрофолатредуктазу и производят на 30-70% меньше метилфолата (синонимы: метафолин, левомефолиевая кислота, метилтетрагидрофолат) чем кто не имеет данную мутацию.
Купить метилкобаламин →
Хотя знание статуса MTHFR очень важно,но оно может не отражать до конца всю клиническую картину. Исследования показывают, что ряд генов, помимо MTHFR, влияют не только на циклы метилирования, но и на вторичные побочные продукты и функцию генов. Такие гены как MTR, MTRR, COMT и AHCY играют важную роль в способности пациента к метилированию.
Мутация в гене MTR (A2756G) приводит к дефициту метилкобаламина. Этот цитоплазматический фермент метионинсинтаза (MTR) катализирует метилирование гомоцистеина с образованием метионина, используя 5-метилтетрагидрофолат.
Реакция протекает путем переноса метильной группы из 5-метилтетрагидрофолата с образованием метилкобаламина и последующим переносом метильной группы из метилкобаламина в гомоцистеин с образованием метионина.
При дефиците метилкобаламина также происходит повышение гомоцистеина в крови.
Купить Витамин В2 →
Ген MTRR кодирует метионинсинтазоредуктазу, фермент, который помогает восстановиться метионинсинтазе (MTR) и дальше превращать кобаламин в метилкобаламин.
Мутация (A66G) в гене MTRR может привести к появлению менее эффективного или совсем неэффективного фермента. Это специфически связано с дефектами нервной трубки, колоректальным раком, сердечно-сосудистыми заболеваниями и повышенным риском синдрома Дауна.
В сочетании с полиморфизмом MTHFR C677T генотипы MTRR AG / GG влияют на общий уровень гомоцистеина в плазме. Кроме того, комбинация генетических полиморфизмов в MTRR и MTHFR была связана с увеличением повреждения ДНК.
Витамин B2 необходим для нормальной работы фермента метилентетрагидрофолатредуктазы (MTHFR).
Купить витамин B6 →
Ген CBS кодирует фермент, называемый цистатион-бета-синтазой. Этот фермент вместе с коферментом витамином B6 необходим для превращения аминокислот гомоцистеина и серина в молекулу, называемую цистатионином.
Затем другой фермент превращает цистатионин в аминокислоту цистеин, которая используется для образования белков и глутатиона. В гене CBS было выявлено более 150 мутаций, вызывающих повышение гомоцистеина в крови.
Наличие мутации в гене CBS приводит также к гомоцистинурии. Выявить гомоцистинурию можно методом тандемной масс-спектрометрии. Такой анализ аминокислот в моче выполняют в российских лабораториях.
Генетические дефекты ферментов фолатного цикла: MTHFR, MTR, MTRR (4 точки) выявляют во многих частных лабораториях, например в KDL.
Метаболический путь синтеза и утилизации гомоцистеина. MTHFR: метилентетрагидрофолатредуктаза; MTRR: метионинсинтдрогеназа.
Диета
Повышение гомоцистеина происходит из-за неправильного питания (отсутствие необходимых пищевых компонентов).
Если человек ежедневно принимает пищу с высоким содержанием белка: мясо, яйца, курица, молоко, то также должен включать в свой рацион определенные жизненно важные аминокислоты. Отсутствие этих жизненно важных аминокислот вызывает гипергомоцистеинемию.
Потребление кофе (4 чашки в день) связано с умеренным повышением гомоцистеина. Строгие вегетарианцы часто подвергаются риску гипергомоцистеинемии из-за низкого уровня B12 в плазме.
Факторы образа жизни
Курение связано с сосудистыми заболеваниями и другими осложнениями, связанными с повышением гомоцистеина. Количество сигарет, выкуриваемых в день, является сильнейшим фактором, определяющим уровень гомоцистеина.
Никотин напрямую влияет на метилирование и катаболизирует фолатный цикл. Недостаточная физическая активность снижает концентрацию общего гомоцистеина в плазме и увеличивает вероятность развития сердечно-сосудистых заболеваний у здоровых и уже больных людей.
Хроническое употребление алкоголя влияет на метаболизм фолиевой кислоты и цианокобаламина. Это связано с желудочно-кишечными нарушениями, которые приводят к снижению поглощения витаминов и фолиевой кислоты, что способствует повышению уровня гомоцистеина.Он также ингибирует метионинсинтазу, чтобы уменьшить поглощение печени и увеличить экскрецию с мочой.
Физическая активность играет важную роль в жизни, так как это самый дешевый способ укрепления нашего здоровья и снижения риска сердечно-сосудистых заболеваний.
Побочный эффект лекарств
Некоторые лекарства, такие как холестирамин и метформин, предотвращают всасывание витаминов из кишечника. Метотрексат, никотиновая кислота влияют на метаболизм фолиевой кислоты, тем самым и на гомоцистеин. Окскарбазепин и топирамат могут вызывать гипергомоцистеинемию из-за их способности активировать печеночные ферменты.
Болезни почек
Пациенты с почечной недостаточностью имеют чрезвычайно высокие уровни гомоцистеина из-за менее эффективного почечного клиренса гомоцистеина.
Пациенты с заболеванием почек имеют высокие показатели сердечно-сосудистой заболеваемости и смерти. Уровни гомоцистеина увеличиваются при снижении функции почек.
Основная причина гипергомоцистеинемии при заболеваниях почек еще не совсем понятна, хотя снижение скорости выведения гомоцистеина почками наиболее вероятная причина.
Распространенность
Распространенность гипергомоцистеинемии широко варьируется в зависимости от географии, пола, этнической принадлежности и возраста. Гомоцистеин повышен среди американского населения у 5-7%, у китайцев — 27,5%, у индийцев — 52-84%. Было установлено, что индийцы имеют более высокий уровень гомоцистеина, чем европейцы.
Легкая гипергомоцистеинемия встречается у 5-7% населения в целом и у 40% пациентов с сосудистыми заболеваниями. В 1990-98 годах смертность от инсульта в США падала на 0,3% в год, но после законодательного обогащения продуктами (фортификации) фолиевой кислотой в 1998 году смертность снизилась до 2,9% в год, что в 10 раз больше.
Частота полиморфизма (мутация в гене MTHFR, ответственного за повышение гомоцистеина) очень мала в некоторых популяциях (
Выявление мутаций в генах, кодирующих ферменты цикла фолиевой кислоты: MTHFR и MTRR
Невынашивание беременности (НБ) – это универсальный интегрированный ответ женского организма на любое неблагополучие здоровья беременной и плода, кумулятивный (интегрированный) ответ на действие неблагоприятных экзогенных и эндогенных факторов.
Проблема невынашивания беременности затрагивает многие семейные пары. Частота невынашивания беременности составляет от 10 до 25% всех беременностей. Решение этой проблемы требует комплексного подхода.
На протяжении последних 50 лет понятие генетические причины НБ включало в себя только наличие хромосомных поломок у супругов и плода.
Но НБ может быть обусловлено и наличием наследственной предрасположенности.
НБ– это результат действия «функционально-ослабленных» вариантов множества генов на фоне неблагоприятных внешних и внутренних факторов.
В настоящее время установлена целесообразность генетического тестирования полиморфизма (мутаций) нескольких генов для установления причин невынашивания беременности:
1) Гены, кодирующие ферменты цикла фолиевой кислоты: MTHFR и MTRR
2) Гены, кодирующие ферменты II фазы детоксикации: GSTMI, GSTTI, GSTPI
Показания к назначению молекулярно-генетического анализа на полиморфизм генов метаболизма (MTRR и MTHFR)
- Рождение в семье ребенка с изолированными пороками пороками нервной трубки, сердца или урогенитального тракта;
- Невынашивание и другие осложнения, связанные с беременностью;
- Плановая подготовка к беременности.
- Выявление у пациента гипергомоцистинемии;
- Наличие у пациента ИБС, артериальной гипертонии;
- Наличие у пациента родственников I и II степени родства ИБС, артериальной гипертонии;
1) Ген метилентетрагидрофолатредуктазы MTHFR C677T
Функция:Фермент является ключевым звеном фолатного цикла и катализирует реакцию превращения гомоцистеина в метионин.
Гомоцистеин — серосодержащая аминокислота, являющаяся продуктом переработки в организме так называемой незаменимой аминокислоты метионина.
Гомоцистеин под воздействием фолиевой кислоты и витамина В-12 возвращается обратно в метионин, или под влиянием витамина В-6 превращается в следующий продукт обмена цистотионин.
Повышение уровня гомоцистеина крови на 5 мкмоль/л приводит к увеличению риска атеросклеротического поражения сосудов на 80% у женщин и на 60% у мужчин.
У людей с повышенным уровнем гомоцистеина повышается риск возникновения болезни Альцгеймера и старческого слабоумия.
При сочетании повышения гомоцистеина крови и сахарного диабета чаще возникают сосудистые осложнения — заболевания периферических сосудов, нефропатия, ретинопатия и др.
Причина повышенного уровня гомоцистеина крови:Вариант С677Т в генеMTHFR-мутация в гене фермента метилентетрагидрофолатредуктазы.
Замена цитозина на тимин в 677 положении приводит к снижению функциональной активности фермента до 35% от среднего значения.
Полиморфизм 677C>T (A223V) широко распространен в различных популяциях и связан по крайней мере с двумя группами многофакторных заболеваний — васкулярными заболеваниями и дефектами развития нервной трубки у плода.
Дефекты в данном гене часто приводят к совершенно различным заболеваниям с широким спектром клинических симптомов: умственное и физическое отставание в развитии, перинатальная смерть, васкулярные и нейродегенеративные заболевания, диабет, рак и другие.Во время беременности в норме уровень гомоцистеина в плазме понижен. Это можно рассматривать, как физиологическую адаптацию организма матери, направленную на поддержание адекватной циркуляции крови в плаценте.
У носителей варианта Т во время беременности наблюдается дефицит фолиевой кислоты, что приводит к дефектам развития нервной трубки у плода.
Курение усугубляет влияние варианта 677T.
Клинические проявления:
- гестоз, преждевременная отслойка нормально расположенной плаценты, задержка внутриутробного развития плода, антенатальная гибель плода;
- дефект развития нервной трубки плода (spina bifida), анэнцефалия, умственная отсталость ребенка, «заячья губа», «волчья пасть»;
- преждевременное развитие сердечно-сосудистых заболеваний (атеросклероз!), артериальные и венозные тромбозы.
Назначение фолиевой кислоты может значительно снизить риск последствий данного варианта полиморфизма
- Данные о полиморфизме:частота встречаемости гомозиготы в популяции – 10-12%
- частота встречаемости гетерозиготы в популяции – 40%
- аутосомно-рецессивное наследование
2) Ген метилентетрагидрофолатредуктазы MTRR 66A->G
Функция:Ген MTRR кодирует фермент редуктазу метионинсинтазы (MTRR), участвующий в большом количестве биохимических реакций, связанных с переносом метильной группы. Одной из функций MTRR является обратное превращение гомоцистеина в метионин. В качестве кофактора в этой реакции принимает участие витамин В12 (кобаламин).
Полиморфизм 66 A->G связан с аминокислотной заменой в молекуле фермента MTRR.
Результат—функциональная активность фермента снижается, что приводит к повышению риска нарушений развития плода — дефектов нервной трубки.
Влияние полиморфизма усугубляется дефицитом витамина В12. При сочетании полиморфизма 66 A->G гена MTRR с полиморфизмом 677C->T в гене MTHFR риск spina bifida увеличивается.
Полиморфизм 66А->G гена MTRR также усиливает гипергомоцистеинемию, вызываемую полиморфизмом 677C->T в гене MTHFR.
Данные о полиморфизме:
Частота встречаемости варианта G полиморфизма в популяции:
- G/G — 15-25%,
- A/G — 40-50%.
- Преобладающий генотип в популяции: (A/G)
Материал для исследования:
венозная кровь, буккальный эпителий
| Кат.№ | Наименование анализа | Сокращенное наименование анализа | Срок выполнения |
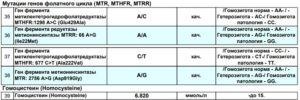
| II.3.8 | Мутация 677C>T метилентетрагидро-фолатредуктазы (MTHFR) | MTHFR 677C>T | 7 дней |
| II.3.9 | Мутация 66A>G редуктазы метионинсинтетазы (MTRR) | MTRR A>G | 7 дней |
Для юридических лиц:
По вопросам сотрудничества с нашей лабораторией Вы можете связаться с нами любым удобным способом:
- По телефону: +7 (383) 334 86 14
- e-mail: info@biolinklab.ru
- C помощью контактной формы:
Физические лица (пациенты) могут пройти данное исследование в обособленном подразделении лаборатории «БиоЛинк» Медицинском центре «Статус» по адресу: г. Новосибирск, ул. Владимировская д. 2/1, тел. +7 (383) 248 90 09.
Мутации генов гемостаза: причины возникновения и коррекция

Гемостаз — одна из важнейших систем организма, которая отвечает за нормальную свертываемость крови и остановку кровотечений. Правильное функционирование этой системы определяет здоровое состояние кровеносных сосудов, сохранение жидкого состояния крови.
В то же время мутации гемостаза могут привести к различным серьезным патологиям, например, развитию тромбозов, сердечно-сосудистых заболеваний, невынашиванию беременности.
О причинах возникновения мутаций и способах их коррекции Medical Note рассказала гемостазиолог Седа Майрабековна Баймурадова — научный руководитель Научного центра гемостаза, тромбоза и фетальной медицины, врач акушер-гинеколог, доктор медицинских наук.
Седа Майрабековна, какие мутации генов гемостаза выделяют в медицине и каковы причины их возникновения?
— В настоящее время к мутациям генов гемостаза относятся мутация FVLeiden, FIIG20210A, дефицит протеина С, дефицит протеина S.
Что же касается причин их возникновения, то отмечу, что мутации генов гемостаза связаны главным образом с наследственным фактором, то есть мы рождаемся с этими генами или полиморфизмами, это то, что мы получили по наследству от своих родителей, они с нами с рождения.
Возможно, природа появления этих мутаций компенсаторная — возмещающая. Кровотечение сопровождает рождение человека, и должен быть механизм внутри человека, который остановит это кровотечение.
Но в ряде случаев тромбофилия (состояние организма, характеризующееся повышенным тромбообразованием) работает как причина серьезных осложнений со здоровьем.
Какие гены гемостаза наиболее часто подвержены мутациям?
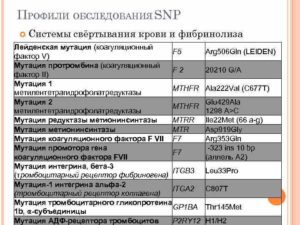
— У каждого четвертого человека в популяции может быть та или иная мутация генов тромбофилии, например, «675 4G/5G» в гене ингибитора активатора плазминогена 1-типа PAI-1, полиморфизм «163G/Т» в гене A-субъединицы фактора XIII, «I/D» в гене тканевого активатора плазминогена, «-455G/A» в гене фибриногена β-субъединицы, «1565 Т/С» в гене гликопротеина Gp-IIIa тромбоцитов, MTHFRC677T.
В чем опасность мутаций гемостаза?
— Наличие мутаций гемостаза является фактором риска внезапных осложнений — тромбозов, инфарктов, инсультов.
У женщин в период беременности мутации гемостаза также могут привести к невынашиванию и угрозе невынашивания, гестозам, способствовать бесплодию.
Кроме того, генетическая предрасположенность к тромбофилии может приводить к возникновению сердечно-сосудистых заболеваний (АГ, атеросклероз, мерцательная аритмия).
В каких случаях необходимо обследование на мутации генов гемостаза?
— Обследование на мутации генов гемостаза показано в следующих случаях:
- при наличии тромбоза, инфаркта или инсульта в анамнезе, если в роду у пациента есть родственники с такими заболеваниями;
- при невынашивании, отягощенном течении беременности (угроза прерывания, гестоз, ПОНРП — преждевременная отслойка нормально расположенной плаценты);
- при бесплодии и неудачах ЭКО.
Возможна ли коррекция мутаций гемостаза во время беременности?
— Да, при условии, что мы знаем, какие мутации и в каких сочетаниях выявлены у пациенток.
Коррекция влияния тромбофилии на организм пациентки возможна двумя способами.
Первый — это традиционное лечение при наличии проблем со здоровьем. Здесь мы назначаем лечение, ориентируясь на результаты анализов и имеющиеся жалобы.
Второй способ — профилактический: на основании только результатов анализов.
Расскажите, пожалуйста, о диагностике и способах коррекции мутаций гемостаза
— Анализ на мутации тромбофилии сдается один раз в жизни, и его результаты не меняются. Соблюдения специальных условий перед сдачей анализа нет, то есть можно сдать кровь на наследственную тромбофилию в течение дня независимо от того, поел пациент или нет.
Обследование помимо стандартной диспансеризации (общий анализ крови и мочи, ЭКГ) должно включать скрининг анализ крови на определение состояния кровотоков-гемостазиограмма +ДДимер, АТ 3, Парус-тест. Этот анализ поможет своевременно выявить скрытую угрозу здоровью пациента и предупредить вышеописанные осложнения.
Вообще, нет единого протокола лечения мутаций тромбофилий.
Принципиально надо понимать, что нельзя лечить результаты анализов. Врач оценивает в первую очередь жалобы пациента, во вторую — результаты обследования. Лечение направлено главным образом на улучшение кровообращения.
Способы лечения тромбофилии разные. Это здоровый образ жизни, правильное питание, прием лекарственных препаратов, применение в некоторых случаях гирудотерапии (оздоровление организма и лечение пиявками), здоровый сон.
Замечу, что наибольший оздоровительный эффект приносит терапия, подобранная индивидуально для каждого пациента.
Лечение может быть курсовое или постоянное в зависимости от причины обследования или жалоб пациента.
Гемостаз крови: что это такое, анализ на мутации и нарушения — Про осуды
Гемостаз является сложным процессом, обеспечивающим жизнеспособность организма. Благодаря ему кровь не может покинуть циркуляторное русло, при этом необходимый объем ее сохраняется. Таким образом поддерживается нормальное кровообращение и снабжение органов кислородом и питанием.
Что это такое?
Гемостаз включает в себя комплекс функционально-морфологических и биологических систем, которые занимаются поддержкой состояния крови в жидком виде, не позволяя ей сворачиваться в рамках закрытой циркуляции. Если нарушена целостность сосудов, то образуется тромб, который закупоривает место повреждения, в результате чего кровотечение останавливается. Основой тромба является фибрин, который удаляется в дальнейшем.
Далее в статье мы разберемся, зачем нужен анализ крови на гемостаз.
Функции
Гемостаз представляет собой комплексную систему, которая выполняет ряд важных функций:
- Помогает крови оставаться в жидком состоянии.
- Свертывает кровь в местах повреждения сосудов, тем самым предотвращая кровотечение.
- Растворяет тромбы. Данный процесс в медицине именуется фибринолизом.
Какой фермент отвечает за свертываемость
За свертываемость крови в нашем организме отвечает 13 ферментов. Такие белки носят название факторов свертывания. Данный процесс проводится в несколько этапов и представляет собой преобразование профермента в фермент (или неактивного фактора в активный). Это запускает цепную реакцию. И такой процесс обычно называется каскадом свертывания.
Он бывает внешним и внутренним. Для последнего все необходимые составляющие уже находятся в составе крови. А для активизации внешнего пути необходим тромбопластин, который является тканевым фактором. В нормальном состоянии его нет, он вырабатывается только в случае повреждений клеток.
Для выявления этого состояния и проводят анализ крови на гемостаз.
Механизмы
У описываемого процесса существует два основных механизма:
- Сосудисто-тромбоцитарный или первичный. В нем принимают участие кровяные клетки, в том числе эритроциты, тромбоциты, а также биоактивные вещества, стенки сосудов и экстраваскулярная ткань. Он обусловлен выработкой специальной пробки для закупоривания повреждения.
- Коагуляционный или вторичный. В данном процессе участвуют плазменные и тканевые факторы свертывания крови. Механизм преобразует фибриноген в фибрин, который не растворяется. Таким образом получается остановить кровотечение в тех сосудах, где оказалось недостаточно первичного механизма. Это происходит в тех случаях, когда сгусток тромбоцитов не смог справиться с повышенным давлением кровотока и необходим больший тромб.
Процесс гемостаза происходит путем взаимодействия таких компонентов структуры, как сосудистые стенки, ферменты плазмы и клетки крови. Во все составные его части входят элементы, которые не позволяют ей сворачиваться, и те, что обеспечивают образование тромба в месте повреждения.
Фибринолиз является механизмом, который отвечает за расщепление фибрина, восстановление проходимости сосудов, поддержание нормальной густоты крови. В составе этой системы плазмин, активатор плазминогена, ингибиторы.
Фибринолиз бывает ферментативным и неферментативным, иногда проходит по внешнему или внутреннему путям активации.Этот процесс основан на способности лейкоцитов к уничтожению и перевариванию патогенных организмов, ликвидации тромбоза и удалению его остатков.
Цель анализа крови на гемостаз
Описываемое исследование проводится с целью выявления нарушений в системе кровообращения. Это довольно сложный анализ, направленный на комплексную оценку всего процесса свертывания в организме человека.
Патологии могут быть с обеих сторон: как в свертывающей, так и в противосвертывающей системе. В последнем случае появляется склонность к развитию геморрагического синдрома, в первом же — к образованию тромбов.
Анализ на гемостаз может выявить тромбофилию – высокую скорость свертываемости крови. Это опасно возникновением бесплодия или невозможности выносить ребенка, а также инфаркта, тромбоза нижних конечностей на фоне варикоза и инсульта.
Низкая свертываемость крови характеризуется кровоточивостью. Таким образом, повреждения заживают очень долго и сложно. Повышается риск послеоперационных осложнений, геморрагического синдрома и внутренних кровотечений.
Как сдавать анализ крови на гемостаз, рассмотрим ниже.
Когда необходимо такое исследование
Необходимость проведения анализа на гемостаз обусловлена следующими ситуациями:
- Диагностика причин возникновения кровоточивости, геморрагической сыпи и кровоизлияний.
- Предотвращение геморрагического синдрома после оперативных вмешательств.
- Выявление, профилактика и терапия инфарктов, инсультов и тромбозов.
- Гинекологические заболевания, планирование беременности, период гестации.
Применяется определеннаясистема расшифровки гемостаза в анализе крови.
Показания к проведению и виды тестов
Чаще всего исследование крови на гемостаз проводят, когда предполагаются большие кровопотери, а также в комплексном обследовании для выявления некоторых заболеваний. Коагулограмма входит в список обследований в следующих случаях:
- в период вынашивания ребенка;
- в пред- и послеоперационный период;
- при тромбозах и венозном расширении вен;
- при аутоиммунных заболеваниях — ревматоидном артрите, красной волчанке, дерматомиозите и т. д.;
- при патологиях печени;
- после инфарктов и инсультов;
- во время терапии антиагрегантами и антикоагулянтами;
- при геморрагическом диатезе;
- в период планирования предстоящей беременности.
Последнее особенно касается женщин с имеющимися в анамнезе гинекологическими заболеваниями, включая бесплодие и невынашивание плода.
Тесты
Анализ на гемостаз заключается в проведении нескольких тестов, а именно:
- МНО — определяется время, за которое сворачивается кровь.
- АЧТВ – время, необходимое, чтобы образовался сгусток после соединения плазмы с реагентами.
- Тромбиновое время – период, за который фибриноген преобразуется в фибрин под воздействием тромбина.
- Фибриноген.
В результате исследования получается коагулограмма, которая требует расшифровки специалистом. Главными показателями являются АЧТВ и МНО, так как именно они демонстрируют активацию по внешнему и по внутреннему пути свертывания крови. Когда они в норме, это говорит об отсутствии серьезных проблем с гемостазом. А какие отклонения выявляет анализ крови на гемостаз?
Нарушения
Если в показателях исследования имеются отклонения от нормы, у пациента могут наблюдаться следующие патологии:
- Когуалопатия. Нарушение функционирования систем свертывания и противосвертывания крови.
- Гипокоагуляционно-геморрагический синдром. Характеризуется пониженным уровнем скопления тромбоцитов, что приводит к снижению показателей активности плазменных и тканевых факторов свертываемости. В результате возникает кровоточивость и геморрагический синдром.
- Гиперкоагуляционно-тромботический синдром. Высокий уровень скопления тромбоцитов и активности плазменных и тканевых факторов свертываемости, что приводит к образованию тромбов.
- Тромбо-геморрагический синдром или ДВС-синдром. Это диссеминированное свертывание крови внутри сосудов с образованием аномального количества тромбов и агрегатов кровяных телец. Как результат, возникает сбой в системе кровообращения, что становится причиной дистрофических патологий.
Исследование на мутации генов
Расшифровка анализа крови на гемостаз не всегда позволяет составить прогноз возможных рисков, связанных с возникновением патологий в области свертываемости у конкретного пациента.
Поэтому проводится дополнительное исследование генов, отвечающих за задействование всей системы, к примеру, при наличии воспалительных процессов и во время беременности.
Показаниями для направления крови на исследование мутаций генов являются:
- Подбор оральных контрацептивов.
- Бесплодие и невозможность выносить плод.
- Заместительное лечение гормональными препаратами.
- Курение пациентами в возрасте младше 50 лет.
- Тромбоз у пациентов младше 50 лет.
- Перед гинекологической операцией, эндопротезированием и трансплантацией.
- Перенесенные инсульты, тромбозы, инфаркты в возрасте младше 50 лет, ТЭЛА. Причем касается это не только самих пациентов, но и их ближайших родственников. Это же правило касается родственников тех, кто умер, не дожив до 50 лет.
- Нарушения слуха невыясненной этиологии.
- После химиотерапии.
Во всех вышеперечисленных случаях существует необходимость исследовать кровь на генные мутации в системе свертывания, а также обмена фолиевой кислоты.
Анализ крови на гемостаз при беременности
Особое место в исследовании на функционирование гемостаза занимают женщины во время беременности. В этот период особенно высок риск увеличения свертываемости крови, что может привести к закупорке сосудов диссеминированного типа. Результатом такого процесса может стать загустевание крови и как следствие нарушение кровоснабжения плаценты.
Вместе с кровью к плоду перестает поступать кислород в достаточном количестве, а также полезные питательные вещества. Возникает аномалия развития ребенка, что заканчивается замиранием беременности или гибелью плода. Своевременная диагностика таких нарушений даст возможность женщине выносить и родить здорового малыша.
Что такое анализ крови на мутации генов гемостаза? Это частый вопрос у беременных. Дело в том, что гемостаз в период гестации может изменяться. Причинами могут стать лишний вес, травмы, стрессы, инфекции хронического характера и онкозаболевания.
Но до наступления беременности женщина может не знать об имеющихся проблемах со свертываемостью.С момента зачатия ее организм претерпевает значительные изменения, связанные с ослаблением защитных характеристик, что и может привести к патологии гемостаза и проявиться тромбозами или кровотечениями.
Такие нарушения могут стать причиной гестоза, анемии, отслойки плаценты и гибели плода. Поэтому для женщины очень важно сдать анализ до беременности либо во время вынашивания. Идеальным вариантом является проверка до зачатия ребенка, во время планирования беременности. Если патологии будут выявлены, то заранее проведенная терапия позволит спокойно выносить и родить здорового малыша.
Чтобы не исказить результаты исследования, за неделю до него нельзя принимать разжижающие кровь препараты и употреблять алкоголь.
Когда показан такой анализ
Есть много ситуаций, когда показан анализ на мутации гемостаза:
Замирание беременности или выкидыш более одного раза. Это может происходить в том числе и по причине плохой свертываемости крови.
Токсикоз, который влияет на вынашивание. Характеризуется повышением артериального давления, отеками и присутствием белка в моче.
Гипертонус матки. Может стать причиной выкидыша.
Отслойка плаценты. Наиболее часто это происходит по причине нарушений в гемостазе. Поэтому требуется обязательная консультация гемостазиолога.
Наличие у родственников проблем в виде инсульта, инфаркта, тромбоза и варикоза.
Бесплодие.
Если во время беременности выявлены нарушения в функционировании гемостаза, назначается терапия, подобранная в индивидуальном порядке. Заключается она в корректировке поврежденного механизма. В первых триместрах беременности подбирается наиболее щадящий вариант медикаментозного лечения.
Как видите, анализ крови на мутации гемостаза информативен и очень необходим для беременных.
Заключение
Гемостаз — это очень важная часть функционирования нашего организма. Самым актуальным исследование крови на свертываемость является в случае беременности и во время планирования зачатия.
Ведь основным моментом вынашивания является беспрерывное кровоснабжение плаценты и питание плода, а в противном случае всегда высок риск развития патологий внутриутробного развития и замирание беременности.
Своевременная диагностика позволит вовремя принять все необходимые меры для спасения будущего ребенка.
Анализ на гемостаз также важен для людей с имеющимися патологиями в системе кровообращения. Им необходимо регулярно сдавать материал на проверку, так как это поможет предотвратить возможные рецидивы заболеваний и держать ситуацию под контролем.
Теперь мы знаем, что показывает анализ крови на гемостаз.
Мутация генов гемостаза: проявления и последствия
Гемостаз – система организма, которая отвечает за нормальную остановку кровотечений и свертываемость крови. Функционирование гемостаза зависит от состояния стенок сосудов, от количества тромбоцитов в крови и некоторых других факторов.
Для мутантов MTRR
Заметила в этом цикле, что если насасывать витамин в12 (у меня такой), яичники сильнее горят, а грудь наливается, особенно во 2 фазе. Причем я его пью в комплексе, но там 100 мкг и он в такой дозировке на меня никак не действует, надо 1000 мкг.
У меня мутация MTRR в гомозиготе, то есть самая сильная, когда организм не имеет фермента, который усваивает В12.Я начала копать, чем полезен вообще витамин В12 для клеток.Если не вырабатывается фермент метилмалонил-КоА-мутаза, то есть его нет, то клетки рождаются не зрелыми.
А так как ячники выпускают постоянно незрелые як, то откуда будет беременность. Цитирую.
Метилмалонил-КоА-мутаза — фермент, необходимый для деления клеток; при блокировке фермента клетка постоянно увеличивает размер ядра (накопляет ДНК), «зреет, но не дозревает» до полного разделения на две независимые клетки; повышается концентрация промежуточного продукта обмена — метилмалоновой кислоты (ММА).
и
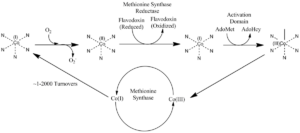
Метионин-синтаза (MTR) — при помощи фолиевой кислоты и витамина В12 гомоцистеин превращается в метионин; таким способом обезвреживается гомоцистеин, высокие уровни которого повреждают сосуды и увеличивают риск сердечно-сосудистых осложнений атеросклероза (инфаркт, инсульт).
Функции витамина B12
- пролиферация всех клеток, особенно клеток крови (они делятся намного чаще)
- синтез генетического материала клетки — ДНК и РНК
- изоляция нервного волокна и проведение импульса
- синтез миелина
- обмен аминокислот
- нейтрализация токсических веществ
Как же проявляется дефицит витамина В12?
- повышенная усталость
- головная боль и головокружение
- сонливость или бессонница
- рассеянность
- одышка и частое сердцебиение
- сильные боли рук и ног
Лабораторный признак недостатка витамина В12 — мегалобластная или макроцитарная (пернициозная) анемия с типичными изменениями в общем анализе крови:
- снижение числа эритроцитов
- снижение уровня гемоглобина
- повышение среднего размера эритроцита — индекса MCV, средней концентрации гемоглобина в эритроците — MCHC, среднего количества гемоглобина в одном эритроците MCH
- сдвиг лейкоцитарной формулы вправо — появление большего числа старых лейкоцитов.
Еще я вычитала такой факт, что если вы пьете витамин в12, он легко определяется в крови анализами, но это не значит, что он есть в клетка тела. Вот как раз развернутые анализы помогают определить насколько сколько его в клетках присутствует в12.
Еще вычитала, если много в организме фолиевой, но мало в12, то все симтомы и анализы сотрутся, то есть будут в норме, но клетки так и не дополучили в12. Смотрим симтомы, если они есть, а анализы в норме, обратите внимание, пьете ли фолиевую.
Стадии дефицита витамина В12
- I — в клетках снижен уровень кобаламина
- II — снижен уровень витамина в крови, ранние последствия отрицательного баланса — повышение гомоцистеина, сниженная скорость синтеза ДНК
- III — видимые метаморфозы в крови, в то же время обратимые изменения нервной ткани
- IV — непоправимые изменения в структуре нервных волокон
3 факта о витамине B12
- в отличие от других витаминов кобаламин способен накапливаться в теле — преимущественно в печени, мышцах, костной ткани и почках
- депо-форма в органах — аденозилкобаламин, в крови — метилкобаламин
- недостаток витамина В12 может быть скрыт приемом препаратов фолиевой кислоты (и, наоборот)
Сниженое всасывание витамина В12 в кишечнике
- пернициозная анемия — антитела к париетальным клеткам желудка или к внутреннему фактору приводят к неспособности витамина В12 присоединиться к своему рецептору на стенке кишечника, таким образом он транзитом проходит по кишечнику
- аутоиммунные реакции против париетальных клеток, внутреннего фактора или комплекса [внутренний фактор+витамин В12]
- хроническая недостаточность ферментов поджелудочной железы, например, при хроническом панкреатите
- синдром Золлингера-Эллисона — повышение продукции гастрина приводит к повышенной кислотности в желудке и в кишечнике, внутренний фактор не может присоединиться к витамину В12
- синдром Имерслунд-Гресбека - редкая рецессивно-наследуемая форма анемии, мутация одного из двух генов кубилина или амнионлес; витамин не проникает через кишечную стенке и теряется с калом
- сниженная кислотность в желудке (ахлоргидрия)
нарушение транспорта витамина В12
- генетические дефекты переносчиков — транскобаламинов
- хронический гранулоцитарный лейкоз
- повреждение эндотелиальных клеток, продуцирующих транспортные белка кобаламина
Повышение поступления витамина В12 в организм не имеет тяжелых последствий, ведь тело способно регулировать как поступление, так и выведение витамина. Описаны единичные случаи передозировки препаратов витамина В12 в виде местной склеродермоидной реакции и аллергии в месте инъекции.
Метилирование и генетическая мутация фермента MTHFR
Ориентировочное время чтения: 7 мин.
Ссылка на статью будет выслана вам на E-mail:
Метилирование является ключевым путем по выводу токсинов из организма. Это происходит за счет того, что токсины любого вида преобразуются в водорастворимые вещества, что позволяет эффективно выводить их из организма.
Налаженный процесс метилирования означает, что у человека больше шансов избавиться от токсинов и тяжелых металлов, что в свою очередь снижает риск развития раковых заболеваний и других проблем со здоровьем.
Перечислим некоторые болезни, связанные с аномальным метилированием: сердечно-сосудистые заболевания, остеопороз, диабет, поведенческие расстройства, расстройства аутистического спектра, синдром дефицита внимания, депрессия, деменция, выкидыш/преждевременные роды, врожденные синдромы, включая синдром Дауна, расщепление – порок позвоночника, расщепление нёба (разг. заячья губа, волчья пасть), дисплазия шейки матки, а также рак шейки матки, кишечника и легких.
Метилирование отвечает за:
- Восстановление РНК и ДНК.
- Регулирование работы иммунной системы.
- Производство глутатиона.
Данное вещество (трипептид) обладает мощными антиоксидантными свойствами и отвечает за выведение из тела различных токсинов и тяжелых металлов, включая: ртуть, свинец, кадмий, мышьяк, никель, олово и алюминий.
- Регулирование воспалительных процессов за счет контроля уровня гомоцистеина. У людей с нарушениями метилирования очень высокий уровень содержания гомоцистеина в крови, что создает для них риск развития сердечно-сосудистых заболеваний.
- Производство специальных белков, подавляющих развитие опухоли (которые действуют вроде переключателей, и могут запустить или прекратить процесс развития рака в организме). Эти белки разрушаются, если нарушен процесс метилирования.
Генетические мутации фермента MTHFR
В гене MTHFR содержится информация по образованию фермента под названием метилентетрагидрофолатредуктаза (MTHFR). Этот фермент принимает участие в расщеплении аминокислот и является важным компонентом в химической реакции, которая задействует витамин В9 (фолат).
Таким образом, этот фермент преобразует 5,10-метилентетрагидрофолат в молекулу под названием 5-метилтетрагидрофолат. Это является необходимым шагом в процессе, в ходе которого гомоцистеин (аминокислота) преобразуется в другую аминокислоту под названием метионин.
Метионин необходим телу для производства белков, работы антиоксидантов и для помощи печени в расщеплении жиров.
Оптимальный уровень фолатов очень важен для нормального протекания многих функций в теле человека, включая: восстановление ДНК, детоксикацию, улучшение настроения, поддержание нормального уровня гомоцистеина, и контроль над воспалительными процессами.
Фолат – естественное, встречающееся в природе вещество, известное как витамин В9, содержится во фруктах, спарже, темно-зеленых листовых овощах, говяжьей печени и цельных злаках.Фолиевая кислота является его синтетическим аналогом и используется при создании витаминных добавок низкого качества, а также при обработке продуктов с намерением предотвратить дефицит питательных веществ.
Фолиева кислота впитывается в организме гораздо быстрее, чем фолат, но в таком случае необходимо преобразование фолиевой кислоты в биологически активную форму прежде, чем организм начнет её использовать.
И если организмы пациентов с генной мутацией фермента MTHFR не способны производить это преобразование, то это может приводить к проблемам. Если этот процесс прекращается, уровень гомоцистеина может взлететь до опасной отметки.
Повышенный уровень гомоцистеина может вызывать ряд хронических заболеваний, включая: атеросклероз, образование тромбов, инсульт, а также когнитивные нарушения, включая деменцию и болезнь Альцгеймера.
По некоторым оценкам, по меньшей мере 40% населения может страдать от той или иной формы мутации фермента MTHFR, что может нарушать процесс метилирования.
При этом у некоторых рас наблюдаются более серьезные нарушения, которые охватывают 21% латиноамериканцев, 6-14% представителей европеоидной расы и 2% потомков африканцев, так как у них наблюдаются мутации, затрагивающие 2 и более аллельных гена.
Даже одного мутировавшего аллельного гена достаточно, чтобы прогнозировать риск развития различных заболеваний.
Что можно предпринять:
- Сделайте генетические тесты на наличие мутаций в ферменте MTHFR, чтобы узнать, есть ли в организме проблемы с выводом токсинов.
- Пересмотрите свои пищевые добавки и убедитесь, что они содержат природную форму витамина В9. Это может быть фолиновая кислота или метилфолат, но не фолиевая кислота.
- В связи с тем, что фермент MTHFR влияет на процесс метилирования, также рекомендуется принимать метилированную форму витамина В12, который известен как метилкобаламин (methylcobalamin), а не широко доступную форму цианкобаламина (cyanocobalamin) (метилкобаламин – одна из форм Витамина B12, которая отличается от цианкобаламина тем, что цианогруппа в нём замещена метильным радикалом). Витамин В12 очень важен для хорошего умственного здоровья, которое попадает в зону риска при мутации фермента MTHFR, наряду с другими факторами, перечисленными выше. Вы можете найти метилированные формы добавок с фолатами и витамином В12 в интернете или в аптеках.
- Вводите пищевые добавки в свой рацион постепенно, чтобы держать под контролем процесс освобождения тела от токсинов.
- Начиная с 1998 года в США и Канаде стали обогащать синтетической фолиевой кислотой хлебную муку, кукурузные хлопья, пасту, рис и другие продукты из злаков. Таких продуктов следует избегать, если у вас есть проблемы с метилированием.
- Следуйте принципам здорового питания, отдавайте предпочтение натуральным и цельным растительным продуктам, например: бобам, чечевице, листовым зеленым овощам, шпинату, авокадо, спарже, брокколи, тропическим фруктам и апельсинам.
- Исключите из рациона рафинированные и обработанные продукты, а также сахар, алкоголь и продукты, содержащие кофеин.
- Уделите внимание очищению пищеварительного тракта. Здесь Вы можете найти полезные советы, как это сделать.
- Избегайте токсичных веществ, используйте средства личной гигиены и бытовую химию из натуральных компонентов. Здесь Вы можете найти некоторые предложения, как это сделать.
- Регулярно проводите процедуры по детоксикации организма, к которым относятся инфракрасная сауна, ванны с горькой английской солью (ее также называют солью Эпсома), массаж тела сухой щеткой, регулярная физическая нагрузка, пост на основе соков, а также процедуры, вызывающие потоотделение. Подробнее прочитать о каждой процедуре можно по ссылке.
- Регулируйте свой уровень стресса. Подробнее читайте об этом по ссылке.
Источник: Cancer Compass – An Alternate Route
Перевод: Марина Уткина специально для МедАльтернатива.инфо
Внимание! Предоставленная информация не является официально признанным методом лечения и несёт общеобразовательный и ознакомительный характер. Мнения, выраженные здесь, могут не совпадать с точкой зрения авторов или сотрудников МедАльтернатива.инфо. Данная информация не может подменить собой советы и назначение врачей. Авторы МедАльтернатива.инфо не отвечают за возможные негативные последствия употребления каких-либо препаратов или применения процедур, описанных в статье/видео. Вопрос о возможности применения описанных средств или методов к своим индивидуальным проблемам читатели/зрители должны решить сами после консультации с лечащим врачом. Диагноз – рак: лечиться или жить? Альтернативный взгляд на онкологию
Чтобы максимально быстро войти в тему альтернативной медицины, а также узнать всю правду о раке и традиционной онкологии, рекомендуем бесплатно почитать на нашем сайте книгу «Диагноз – рак: лечиться или жить. Альтернативный взгляд на онкологию»
Читать бесплатно
Мы распространяем правду и знания. Если вы считаете нашу работу полезной и готовы оказать финансовую помощь, то вы можете перевести любую посильную для вас сумму. Это поможет распространению правдивой информации о раке и других болезнях и может спасти чьи-то жизни. Участвуйте в этом важном деле помощи людям!
